

罗婷教授
四川大学华西医院乳腺疾病临床研究中心/肿瘤科 副教授 硕士生导师
中华医学会肿瘤学分会乳腺肿瘤学组青年委员
四川省国际医学交流促进会乳腺肿瘤专业委员会副主任委员
四川省医师协会乳腺专业分会常委,青委会副主任委员
四川省抗癌协会乳腺癌专委会青委副主任委员
四川省预防医学会乳腺疾病控制与预防分会委员
HER2阳性早期乳腺癌患者新辅助治疗后获得病理学完全缓解(pCR),其术后复发风险显著低于未达到pCR的患者[1]。已有多项研究证实,抗HER2双靶方案可显著提高此类患者的pCR率[2-4]。然而,目前批准用于新辅助治疗的抗HER2靶向药物较少,临床需求未满足。因此,亟待在HER2阳性乳腺癌新辅助治疗领域开发更多新的抗HER2靶向药物。
吡咯替尼是由中国原创研发的小分子TKI类抗HER2药物,已证实其在HER2阳性晚期乳腺癌患者中的疗效显著,从作用机制上,吡咯替尼可联合大分子单抗曲妥珠单抗,通过里应外合,胞外胞内协同抗HER2。新一代紫杉醇制剂白蛋白紫杉醇解决了溶解性问题,其疗效更佳,也已在临床广泛使用。因此该研究[5]旨在探索吡咯替尼联合白蛋白紫杉醇和曲妥珠单抗在HER2阳性早期或局部晚期乳腺癌新辅助治疗中的疗效和安全性。
在这项开放标签的Ⅱ期临床研究中,入组患者均为初治的HER2阳性早期或局部晚期乳腺癌患者(临床ⅡA~ⅢC期),给予以下新辅助方案:吡咯替尼400 mg,qd;白蛋白结合紫杉醇125mg/m2,qw,D1/8/15;曲妥珠单抗2mg/kg(首次剂量4mg/kg) qw,D1;共4个周期(q3w为1个周期)。患者术后辅助治疗为4个周期的表柔比星+环磷酰胺+医生选择的抗HER2靶向治疗。研究主要终点为pCR (ypT0/Tis ypN0)。次要终点为ORR(RECIST 1.1)和安全性、耐受性等。
 图1. 研究设计
图1. 研究设计
研究于2019年5月17日至2019年11月26日期间共入组了21例患者,中位年龄48 (28-57)岁,入组患者基线特征见表1。从表中可见,该研究入组患者大部分肿瘤负荷大,临床分期晚,复发风险高。其中T4期比例为52.4%(n=11),N1-3为90.5%(n=19),Ⅲ期为81.0%(n=17),HR阴性为61.9%(n=13),Ki-67≥30%为71.4%(n=15)。
表1. 患者基线特征
总体人群tpCR (ypT0/Tis ypN0)为57.1% (12/21),其中HR阴性亚组的tpCR在数值上明显高于HR阳性亚组(69.2% vs 37.5%,卡方检验P>0.05)。新辅助治疗2周期时,100%患者可达临床缓解;治疗结束时临床缓解仍持续,ORR为100%。
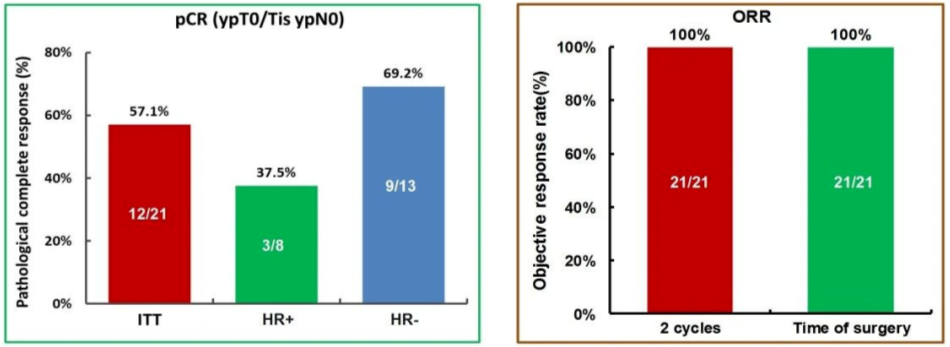 图2. 不同人群的pCR(左)和不同节点的ORR(右)
图2. 不同人群的pCR(左)和不同节点的ORR(右)
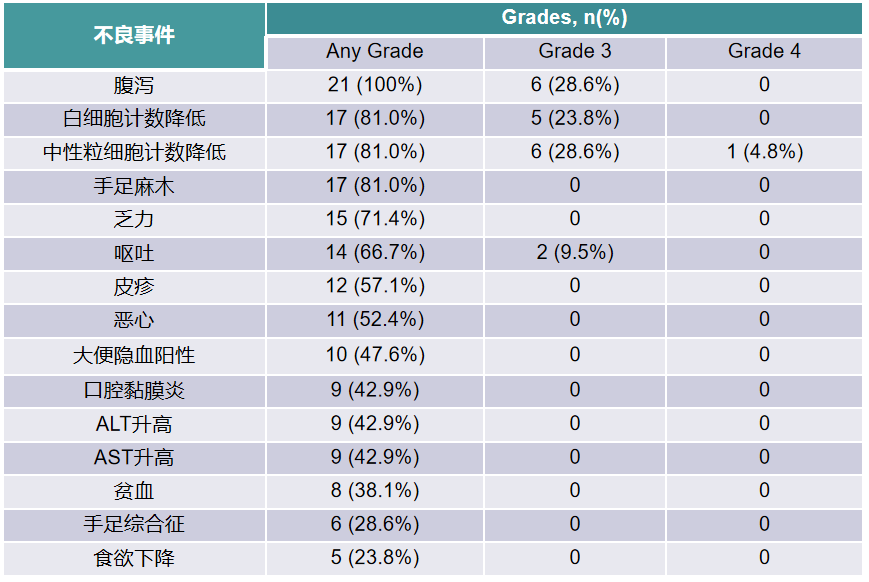
腹泻是最常见的不良事件(AEs),≥3级的发生率为28.6%,无4级腹泻发生,总体可控;≥3级中性粒细胞计数降低的发生率为33.3%,仅有1例(4.8%)患者为4级;无心脏毒性事件发生。
表2. 治疗相关不良事件
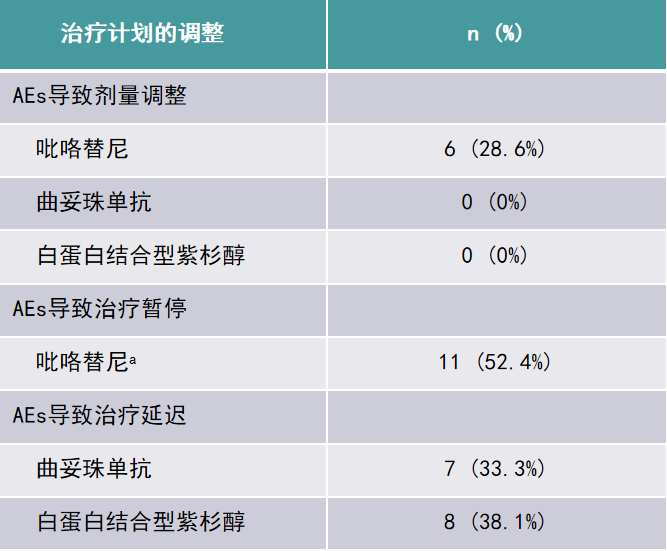
20例(95.2%)患者完成了所有新辅助疗程的治疗(仅1例患者因非AEs原因自行退出);因AEs导致吡咯替尼剂量调整的有6例(28.6%),因AEs导致吡咯替尼治疗暂停的有11例(52.4%),但累计暂停时间较短,中位累计暂停时间为7天(1-24)天;因AEs导致曲妥珠单抗和白蛋白紫杉醇治疗延迟的分别有7例(33.3%)和8例(38.1%),但治疗延迟考虑与白紫周疗引起的AEs相关。
表3. AEs对新辅助治疗的影响
这项研究为早期或局部晚期HER2阳性乳腺癌的吡咯替尼新辅助治疗提供了初步的证据,其结果显示,吡咯替尼联合白蛋白紫杉醇和曲妥珠单抗新辅助治疗可有效提高pCR率,并表现出可接受、可控制的安全性和耐受性。
与既往同类研究横向非头对头比较,NeoSphere[2]和PEONY[3]研究新辅助4周期THP方案的tpCR率均为39.3%,NeoALTTO研究新辅助6+12周HL-THL方案的tpCR率为46.8%[4],而这项单臂研究新辅助4周期吡咯替尼+曲妥珠单抗双靶方案也表现不俗,tpCR率达到了57.1%[5],提示小分子TKI吡咯替尼联合大分子曲妥珠单抗新辅助治疗具有潜在优势,值得进一步扩大样本量的研究进行验证。